거시상태(macrostate)와 미시상태(microstate)Ⅱ
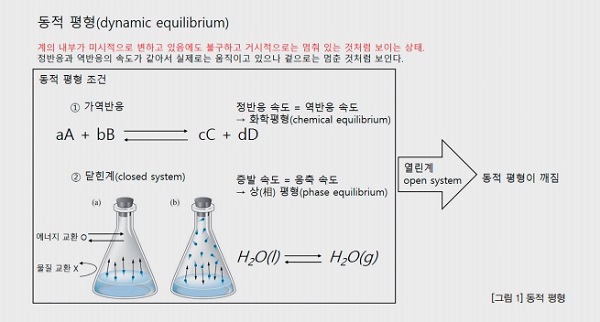
화학 및 물리에서 동적 평형(dynamic equilibrium)은 닫힌계(closed system)에서 일어나는 가역반응이다. 정반응과 역반응 속도가 같고, 혼합물의 조성이 시간에 따라 변하지 않는 경우 닫힌계는 열역학적 평형(thermodynamic equilibrium)이 된다. 이 때 A, B, C, D의 농도는 변하지 않지만 반응은 여전히 양방향으로 발생한다.
평형상수(equilibrium constant, Keq)는 동적 평형에서 반응 지수의 값으로 다음과 같이 정의한다.
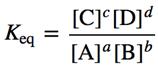
여기서 [A]는 A 물질의 몰 농도이고, 화학 반응식의 계수인 a, b, c, d는 평형상수에서 지수가 된다. 평형상수는 주어진 온도에서 주어진 반응에 대한 특성 수치이고, 반응물과 생성물의 농도와 관련이 있다. 그리고 온도, 용매 및 이온 강도와 같은 반응 변수는 평형상수 값에 영향을 미친다.
평형상수에 대한 지식은 혈액에서 헤모글로빈의 산소 수송과 인체의 산-염기 항상성과 같은 생화학 과정을 이해하는데 필수이다.
1) 물의 자가 이온화(self-ionization of water)
순수한 물의 전기 전도도는 0.055μS/cm이다. 이것은 물에 존재하는 이온 때문이다. 물의 자가 이온화(또는 물의 자동 해리)는 순수한 물의 이온화 반응으로 물 분자(H2O)는 수소 핵 하나를 잃고 수산화이온(OH-)이 되고, 수소 핵(또는 수소이온 H+)은 즉시 다른 물 분자와 결합하여 하이드로늄 이온(hydronium ion, H3O+)을 형성한다. 이것을 자체양성자이전반응(autoprotolysis)의 예이며 물의 양쪽성 특징을 설명한다. 물의 운동에너지(브라운 운동)는 끊임없이 물 분자간의 충돌을 일으키고 물 분자의 해리가 일어난다.
물의 이온화 반응은 흡열반응으로 온도가 증가할수록 물의 이온화가 증가한다. 즉, 온도의 증가는 물의 운동에너지를 증가시키고, 물이 충돌하면서 물의 해리가 증가한다.
![[그림2] 물의 자가 이온화](https://cdn.kmpnews.co.kr/news/photo/202010/40234_35507_1940.jpg)
([그림2] 참고) 순수한 물이 하이드로늄 이온과 수산화이온을 형성할 때 물의 평형상수(Keq)는 1.8×10-16mol이 되고, 평형상수에 물의 몰농도(55.56M)를 곱하면 물의 이온화상수(Kw)는 1×10-14(mol/L)2이 된다. 그리고 물은 하이드로늄 이온과 수산화이온이 절반씩 차지하기에 물의 pH는 7, pOH도 7이 되고, 물은 산성도 염기성도 아닌 중성이 된다. 물의 이온화는 상수(어느 관계를 통하여 변하지 않는 일정한 값을 가진 수나 양)이다. 그렇기 때문에 수소이온이 감소하면 수산화이온이 증가하여서 물의 이온화 상수를 맞추게 된다.
2) 인체의 pH와 완충계
① 아미노산과 pH
중성 pH에서 아미노산의 카르복실기(carboxyl group)는 음전하로, 아미노기(amino group)는 양전하로 하전 된다. 중성 용액에 측쇄에 하전 그룹이 없는 아미노산은 순전하가 없는 양성이온(zwitterion)으로 존재한다.([그림3] 참고)
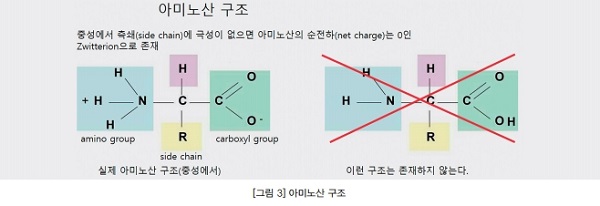
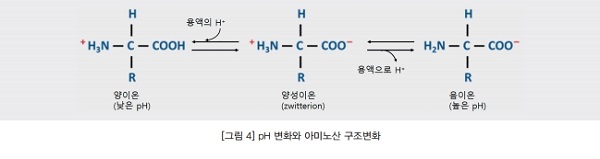
인체의 대사는 최적의 pH에서 작동하고, 생체 분자는 특정 pH 범위에서만 안정적이다. pH를 포함한 상태의 변화에 단백질은 쉽게 변성될 수 있고, 그림4와 같이 다른 부위가 양성자화(protonated, H+의 첨가) 또는 탈양성자화(deprotonated, H+의 제거) 될 때 정전기 상호작용 및 단백질 사슬에 따라 상호작용을 변화시킨다.
② 완충계(buffer system)
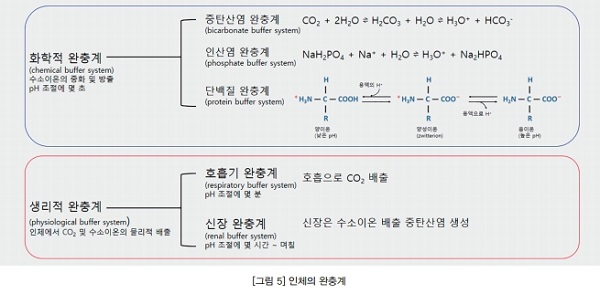
pH 균형을 최적의 수준으로 유지하기 위한 생물한적 시스템인 완충계를 가지고 있다. 완충계는 pH가 변하지 않도록 양성자(H+)를 흡수하거나 제공할 수 있는 화합물을 포함하고 있고, 생리적 완충계는 인체에서 발생한 이산화탄소 및 수소이온을 배출하는 역할을 한다. 즉, 화학적 완충계는 순간적인 pH의 변화를 막아주고, 생리적 완충계는 많은 대사에서 발생하는 산(CO2, H+)을 물리적으로 제거하는 역할을 한다.
3) 생명은 통제된 불균형이다
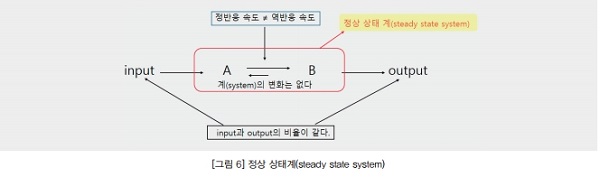
① 정상 상태(steady state)
계(system)의 동작이나 내부속성이 시간에 따라 변하지 않는 경우 정상 상태(steady state)라고 한다. 평형은 닫힌계(closed system)의 특징이라면 정상 상태는 열린계(open system)에서 물질의 출입에도 불구하고 계의 변화가 없는 것이다. 정상 상태 계의 대표적인 예는 생명체이다. 생명체는 외부와 에너지 및 물질을 교환(동적 평형과 다름)하지만 거시상태(흔히 항상성이라고 함)는 변하지 않는다.
② 생명
생명에 대한 정의의 일부는 생명체가 주위 환경과 평형을 이루지 않는 것이다. 체온은 주변 온도와 동일하지 않고, 가장 단순한 것조차 환경과 어느 정도의 불균형을 유지한다. 생명이 살아 있는 동안에는 환경과 불균형 상태에 있지만 생명의 내부 상태는 항상성이라는 평형을 가지고 있다. 외부와 내부가 다르다는 것은 일을 했다는 것이다. 일을 할 때는 반드시 에너지가 필요하다.
인체의 에너지 생성을 TCA cycle부터 살펴보면 TCA cycle의 순 반응은 아래와 같이 볼 수 있다.
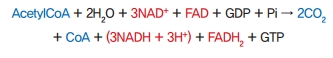
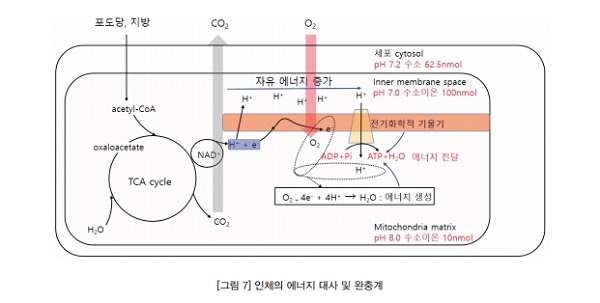
외부 에너지(포도당, 지방 등)는 acetyl-CoA 형태로 TCA cycle로 들어가고, acetyl-CoA와 물을 분해해서 조효소 NAD+, FAD에 수소(H+, e-)를 전달한다. 전자전달계는 분리된 수소를 수소이온과 전자로 나누고 산화환원반응을 통해 이동시키면서 수소와 전자의 전위차 및 자유에너지를 증가시킨다. 이 과정은 ATP 합성효소(ATP synthase)를 통해 ATP 합성에 가능한 에너지를 제공하고, 전자와 수소이온은 산소와 결합하여 물이 된다.
즉, 우리가 섭취하는 영양소의 기본 구조는 (C(H2O))n이고 여기에 물을 가수분해하여 CO2와 수소(H)로 분리한다. 수소는 전자전달계(산화환원반응)에서 수소이온가 전자로 분리가 되고, 마지막에 산소와 결합하여 인체에 필요한 에너지(ATP)를 제공한다.
③ 생명은 불균형을 유지한다
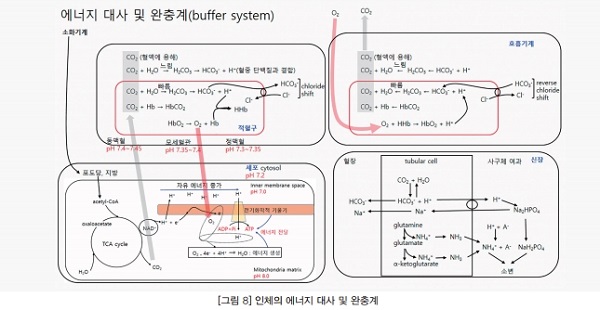
에너지 생성을 위해 인체는 영양소를 흡수해야 한다. 하지만 이것보다 더 중요한 것은 불균형을 유지하는 것이다. 미토콘드리아 매트릭스는 pH 8.0이고, 미토콘드리아 사이막 공간은 pH 7.0이다. 수소이온 농도로 본다면 10배의 차이가 나고, 이 차이가 무너진다면 ATP 생성은 불가능해진다.
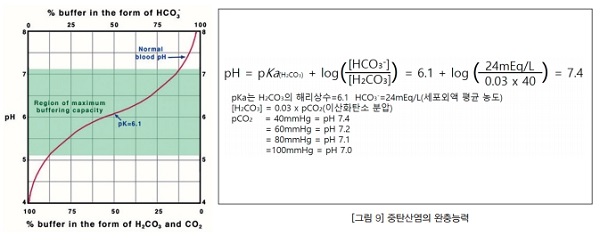
미토콘드리아에서의 수소이온 농도 차이를 설명하기 힘들지만 인체는 호흡기계를 통해 이산화탄소(CO2)를 배설하고, 신장은 수소이온(H+)을 제거한다. 이것으로 중탄산염의 완충능력(그림9참고, pH 6.1을 전후) 보다 높은 혈중 pH 7.4(중탄산염 : 탄산 = 20 : 1, 물의 자동해리로 생성되는 수소이온(100nmol)보다 더 적은 수소이온(40nmol)을 가능하게 함)를 가능하게 한다.
신장을 통한 수소이온의 제거는 인산염(HPO4-)과 암모니아(NH3)를 이용해서 소변으로 내보낸다. 문제는 인산염(뼈의 주요성분)과 암모니아(단백질에서 유래)는 인체의 구성성분이라는 것이다. 혈중 pH 7.4로 거시상태에 문제가 없다고 하더라도 미시상태에서 뼈와 단백질에 아무 문제가 없다는 것은 아니다. 인산염 완충계와 단백질 완충계가 pH를 조절하는 주요 화합물이면서 인체의 구조와 기능에 필수적인 요소라는 것이다.
즉, 인체의 pH 7.4라는 의미는 작은 수소이온의 변화에도 인산염과 단백질에 손상을 일으킨다는 것이고, 생명은 에너지 생성 외에도 동화반응에도 많은 물질 소모가 필요하다는 것을 의미한다.
④ 거시상태와 미시상태
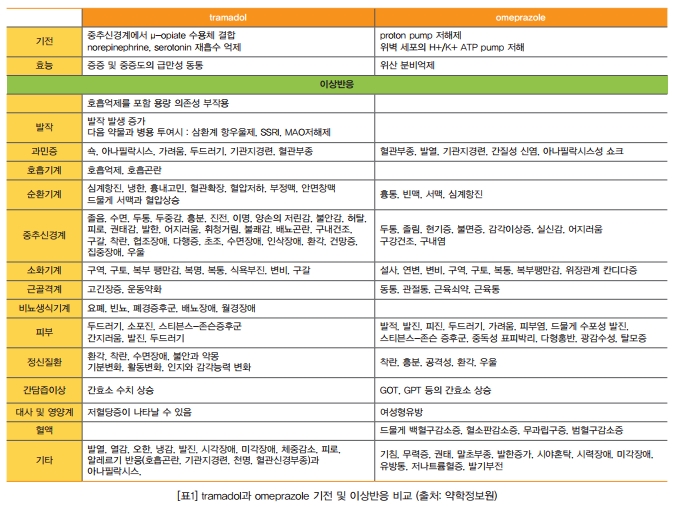
트라마돌(tramadol)은 μ-opiate 수용체 결합을 통해 통증을 억제하고, 오메프라졸(omeprazole)은 위벽 세포의 H+/K+ ATP pump 저해를 통해 위산을 감소시켜 위의 염증 상태를 줄여준다. 하지만 두 약물 모두 조금 다르지만 비슷한 이상반응을 가지고 있다. 트라마돌은 호흡을 억제하여 이산화탄소의 배출을 감소시키고, 오메프라졸은 위산으로 배출되는 수소이온을 억제한다. 호흡의 억제 및 수소이온 배출의 억제는 산증을 유발하고, 표1에 있는 것처럼 다양한 산증과 관련된 반응이 나타나는 것이다.
우리는 다양한 증상에 다양한 약물을 투약한다. 하지만 거시상태만 보고 미시상태의 변화를 이해하지 못하고 약물을 투약한다면 측정 가능한 거시상태만 개선할 뿐 환자가 호소하는 다양한 증상을 개선할 방법은 없게 된다. 우리가 아는 완충계도 인체의 일부이다. 비록 완충계의 변화는 눈에 보이지 않지만 다른 것과 마찬가지로 한계를 가지고 있다. 완충계의 능력을 벗어날 때 산증 및 알칼리증이라 부르지만 그 시작은 이미 오래전에 시작한 것이고, 우리는 그 작은 차이를 반드시 알고 있어야 한다.
참고문헌
NCBI : Science review: Extracellular acidosis and the immune response: clinical and physiologic implications
Introductory Chemistry – 1st Canadian Edition ; The Equilibrium Constant
위키피디아 검색 ; dynamic equilibrium, equilibrium constant
Introductory chemistry 5th edition, Nivaldo J. Tro Chapter 15, Chemical equilibrium, Dr. Sylvia Esjornson Southwestern Oklahoma State University Weatherford, OK


