의약품안전사용서비스(DUR, Drug Utilization Review)는 의료 현장에서 처방이나 조제시 사용하는 시스템으로, 의약품의 처방이 적절하고 의학적으로 필요한 의약품 사용과 부적절한 의학적 사용을 방지하고 있다.
식약처는 10일 고시를 개정해 이 의약품안전사용서비스(DUR)에 병용금지, 임부금지 등 45개 성분을 추가하고 3개 성분에 대해 임부금지 해제했다.
식품의약품안전처(처장 이의경)는 7월 10일 의료현장에서 처방·조제 시 사용하는 ‘의약품안전사용서비스(DUR)’의 ‘의약품적정사용정보’에 병용금기 성분 등을 추가·해제하기 위해 식약처 고시인 '의약품 병용금기 성분 등의 지정에 관한 규정'를 개정했다.
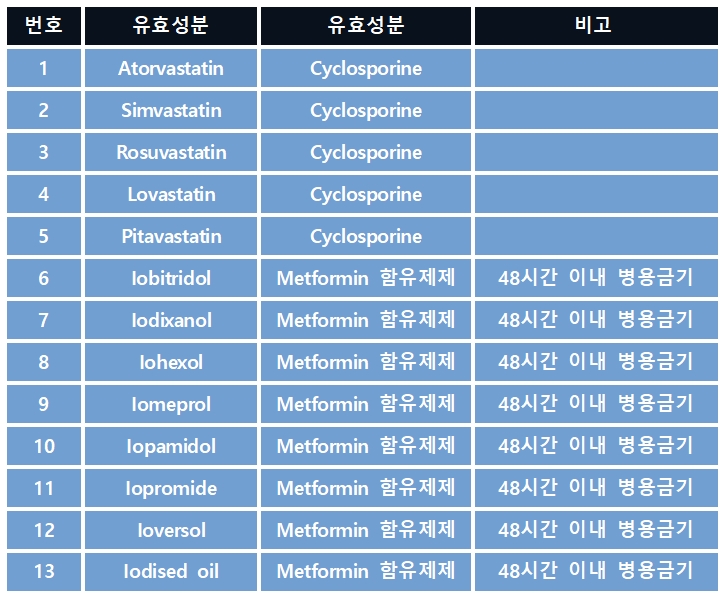
이번 고시로 인해 ‘아토르바스타틴·사이클로스포린’ 등 13개 성분이 병용금지 성분으로 분류되고 ‘테오필린’ 등 32개 성분이 임부금지성분으로 지정되며, 그동안 임부금지 성분이었던 ‘인슐린아스파트’ 등 3개 성분은 임부금지 성분에서 해제됐다.

식약처는 “앞으로도 의료현장에서 의약품이 적정하게 사용될 수 있도록 병용금기, 임부금기, 연령금기 등의 정보를 지속적으로 개발할 계획이며, 의약품 안전사용을 위한 기반이 확대되도록 더욱 노력하겠다”고 밝혔다.
이번 개정 고시 내용은 식약처 홈페이지(www.mfds.go.kr) → 법령정보 → 제·개정 고시 등에서 확인이 가능하다.

