인구고령화로 인해 각종 만성질환 및 치매와 같은 노인성 질환 환자가 증가하고 있다. 이에 본 강연에서는 치매에 대해 살펴보고, 특히 당뇨병 환자의 치매 위험과 관리에 초점을 맞춰 어떤 약제를 사용해 치료를 하는 것이 바람직할지 살펴보았다(편집자 주).
좌장: 김성래(가톨릭의대)
연자: 조광욱(가톨릭의대)
패널: 박경선(김포우리병원), 손장원(부천성모병원), 목지오(부천순천향병원), 김조은(뉴고려병원)
제2형 당뇨병과 치매 - 가톨릭대학교 조광욱

치매는 뇌조직 위축과 함께 기억력 및 인지기능 장애가 동반되면서 발생하는 일상생활 (activities of daily living, ADL)의 장애를 말하는 것으로, 실제적으로 일상생활의 장애가 없으면 경도인지장애 (mild cognitive impairment, MCI)로 진단하고 일상생활의 장애가 있어야 치매로 진단한다.
치매의 종류에는 알츠하이머 치매, 혈관성 치매, 루이체병 치매, 전측두엽 치매가 있으며, 미국과 유럽의 서구권은 알츠하이머 치매가 우세하고, 우리나라와 중국, 일본을 포함한 아시아에서는 알츠하이머 치매와 혈관성 치매가 비슷한 비중을 보이지만, 최근 들어 우리나라는 뇌졸중 환자가 증가하면서 혈관성 치매가 우세한 경향을 보인다 그러나 신경과나 정신과에서는 피질하 혈관성 치매는 알츠하이머병과 감별이 매우 어렵고 이러한 치매는 알츠하이머병의 아형이지 혈관성 치매가 아니므로 혈관성 치매라는 것은 없다고 주장하기도 한다.
중증 치매는 전문적인 치료가 필요하지만, MCI까지는 내분비내과에서도 충분히 관리할 수 있으므로 관심을 가지고 치료할 필요가 있다. 즉, 기억력 저하를 호소하나 일상생활에는 장애가 없고, MMSE (mini-mental state examination)와 같은 객관적 검사에서는 실제로 기억력 저하가 있지만 치매에는 합당하지 않는 상태가 MCI로서, 매년 약 10~15%가 알츠하이머병으로 진행하고 6년 후에는 80% 정도가 알츠하이머병으로 진행하는 고위험군이다. 아직까지 치매는 치료가 불가능하기 때문에 조기진단을 통해 치매로의 진행을 억제하여 가능한 한 오랫동안 일상적인 생활을 유지할 수 있도록 하는 것이 중요하다.
특히 당뇨병 환자를 20년간 추적관찰한 코호트 연구에 의하면, 유병기간이 길수록 인지기능이 유의하게 감소하는 것으로 보고되었다. 즉, 인지기능 감소로 식사조절이나 복약에 대한 순응도가 감소하면, 혈당조절이 악화되는 악의 고리가 활성화되면서 저혈당증까지 동반될 수 있으므로, 당뇨병 치료에서는 인지기능 변화도 주의 깊게 살펴볼 필요가 있다.
사실 치매를 유발할 수 있는 원인질환으로는 여러 가지가 있기 때문에 반드시 혈액검사와 영상검사를 기반으로 진단을 해야 한다. 일례로, 뇌농양이나 뇌출혈도 초기에는 치매와 유사한 증상을 보이지만, 치매와 달리 조기에 적절한 치료를 하면 충분히 치료가 가능하다. 따라서 첫 진단을 내릴 때에는 가능한 한 여러 가지 검사를 진행하여 정확한 진단을 하는 것이 중요하다.
치매진단에 도움을 주는 검사
혈액검사와 영상검사 외에 유전자 검사도 도움을 준다. 한국인에서는 Apo E genotype ε3/ε3가 가장 많고 (72.1%), 그 다음이 ε3/ε4로 알려졌다 (17.1%). MMSE는 1975년 Folstein 이 만든 검사로, 이를 번역한 한국어판이 1989년 도입되었다. 진단검사는 아니며, 검사 시행 지침을 숙지하기 용이하며 5-10분 정도의 짧은 시간에 시행할 수 있는 장점으로 인해 일차적인 선별목적으로 가장 널리 쓰이고 있으며, 특히 치매진단 후 추적검사로서 활용도가 우수하다.
다만 검사 항목 중 읽기와 쓰기, 사칙연산이 있는데, 일부 고령자 중에는 학교교육을 제대로 받지 못해 읽기와 쓰기를 할 줄 모르는 환자도 있으므로, 무학 대상자에게는 가산점을 부여하는 방식으로 점수를 보정할 필요가 있다. 이처럼 MMSE는 연령, 교육수준의 영향을 많이 받기 때문에 교육수준이 낮거나 언어장애가 있는 경우 시행이 어려우며, 뇌 혈관성 치매에 민감하지 않다. 또한 MCI를 감별에는 44-68%의 민감도를 나타내어 초기 단계의 치매 선별검사 도구로 쓰기에는 제한점이 있다.
알츠하이머병과 혈관성 치매의 병태생리
뇌는 여러 뉴런의 연결로 작동하는 기관으로, 뉴런 간 연결은 시냅스를 통해 이루어진다. 즉, 시냅스를 통해 신경전달물질이 전송되면서 인지기능이 유지되는데, 치매와 직접적인 관련이 있는 신경전달물질로 acetylcholine이 있다. 이 외에 연결부위가 모두 끊어진 뉴런의 체부를 말하는 tangle과 단백질 덩어리가 뭉쳐진 plaque도 치매에서 중요한 역할을 한다. 정상 뉴런은 신경섬유 내 미세소관 (microtubules)이 있으며, tau protein은 이들 미세소관을 단단하게 결합시킨다. 하지만 뉴런이 손상되면 이러한 tau protein이 뉴런 내에 침착하는데 이것이 바로 tau tangle이며, 뉴런 바깥쪽에 손상된 뉴런의 기능을 대신할 수 있는 β-amyloid precursor protein이 깨지면서 뭉쳐진 덩어리를 β-amyloid plaque라 한다.
아직까지는 치매를 유발하는 병태생리(노화, 유전자, β-amyloid protein, tau protein, free radical) 중 의학적 중재로 그 변화를 역전시킬 수 있는 방법이 없기 때문에 치매는 불치의 병이지만, 진행을 저해할 수는 있으므로 조기진단을 통한 진행억제가 최선의 치료라 할 수 있다. 현재 β-amyloid protein이나 tau protein이 뇌에 축적되지 않고 분해 및 흡수될 수 있도록 하거나, 이들 물질을 표적으로 하는 면역요법이 치매 치료법으로 연구되고 있다.
혈관성 치매는 뇌졸중 발생 후 동반되며, 다음과 같은 특징을 보인다. 뇌졸중과 같이 치매도 갑자기 발병하며 (abrupt onset), 경과 또한 일정치 않고 변화가 심하며 (fluctuation), 보행장애, 편마비와 같은 신경학적 증상을 동반한다. 모든 뇌졸중이 치매로 진행하는 것은 아니며, 우리나라의 경우 20%는 혈관성 치매로, 48.9%가 MCI로 진행하는 것으로 알려졌다.
따라서 뇌졸중 환자의 70% 정도는 인지기능 손상을 동반한 치매로 발전할 수 있음을 염두에 두고 관리해야 한다. 발생 기전과 양상에 따라 다발성 뇌경색 치매 (multi-infarct dementia)는 다수의 커다란 혈관이 막힌 다발성 뇌경색 후 3개월 이내 인지장애가 동반되며, 악화와 호전을 반복하면서 계단식 진행양상으로 악화된다. 이러한 경우 특히 당뇨병과 같은 위험인자 관리가 중요하다.
뇌졸중 환자의 인지기능 손상을 예방하기 위해서는 이차 예방이 가장 효과적이며 (Circulation 2013;128:1341-1348), 이에 관한 논문들도 많다. 이와 달리 전략적 뇌경색 치매라고도 하는 단일 뇌경 치매 (single infarct dementia)는 치료를 잘 했음에도 불구하고 중요부위 (thalamus, Lt. int. capsule genu, caudate neucleus) 손상으로 인해 영구적 장애를 동반한다.
최근 들어 화두가 되는 것이 바로 피질하 혈관성 치매(subcortical vascular dementia)로, 혈관성 치매로 분류되지만 알츠하이머병과 감별이 어려운 치매이다. 초기단계에서는 작은 혈관이 막혀 작은 경색들이 생기는데, 이러한 경색이 미세혈관 손상에 의한 것인지 아니면 β-amyloid protein이나 tau protein이 뇌에 축적되면서 보이는 신호인지 감별이 어렵고, 병이 더 진행되면 뇌실 주위로 하얗게 손상된 MRI 소견을 보인다. 하지만 대부분의 환자들이 병이 많이 진행된 후에야 검사를 받기 때문에 초기단계에서 발견은 어렵고 이러한 분류에 대해서도 논란이 있다. 과거에는 피질하 혈관성 치매의 발병 원인이 혈관 이상에 의한 것인지 β-amyloid protein이나 tau protein에 의한 것인지 알 수가 없었지만 현재는 amyloid PET라는 영상검사를 통해 알츠하이머병과 혈관성 치매를 감별할 수 있지만 방사선동위원소를 사용하는 고가의 검사이고, 감별 후 치료방법이 달라지는 것도 아니기 때문에 임상연구 목적으로만 시행되고 현실적으로는 거의 시행하지 않고 있다.
치매 치료제
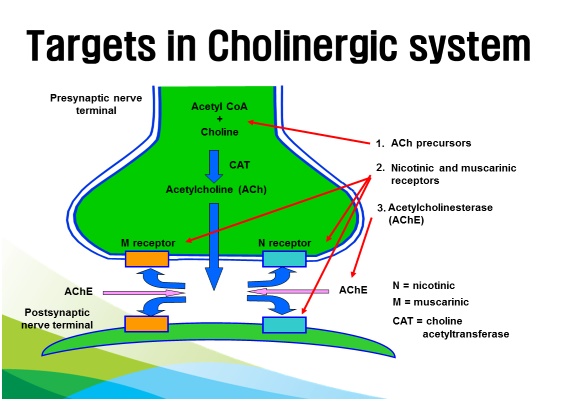
치매에서 cholinergic pathway, 대뇌피질, 해마가 중요한 역할을 하는데, 이들 세 가지가 제대로 작동하기 위해서는 모두 많은 에너지를 필요로 한다. 따라서 저혈당성 코마 혹은 간헐적 저혈당증에 빠진 환자들은 이들 기관이 쉽게 손상되며, 혈압에도 민감하기 때문에 과도한 혈압강하는 만성적 허혈을 초래할 수 있어, 당뇨병과 고혈압 환자의 조절목표에 대해서는 아직도 논란이 계속되고 있다. 특히 치매에서 중요한 역할을 하는 cholinergic pathway가설을 근거로 acetylcholine 분비를 증가시키자는 것이 치료의 표적이 되었다(그림). 즉, 프리시냅스에서 acetylcholine의 분비를 증가시키는 콜린 전구물질 투여를 비롯해, acetylcholine 분비 후 분해되어 수용체를 통해 흡수되는데 분해하는 효소를 차단하여 acetylcholine 농도를 증가시키는 방법, 재흡수와 관련된 니코틴 혹은 무스카리닉 수용체 기능항진에 착안하여 약제들이 개발되었다.
현재 치매치료에 cholinesterase 억제제 (donepezil, rivastigmine, galantamine)와 NMDA 수용체 길항제 (memantine)가 많이 처방되고 있으나, 이들 약제들은 보험급여 인정을 받기 위해서는 MMSE나 CDR, GDS 검사를 해야 하는 번거로움이 있으며, 약물이 뇌에만 작용하는 것이 아니라 근육이나 장에도 작용하기 때문에 부작용 (구역, 설사, 식욕감퇴, 체중감소, 어지러움, 근육경련)이 심하다. 또한 시간이 지날수록 내성을 보이기 때문에 부작용에도 불구하고 증량을 해야 하며, 85세 이상 초고령자, 서맥, 기관지 천식, COPD (chronic obstructive pulmonary disease) 환자에서는 사용이 제한된다는 한계가 있다. 이들 약물 외에 치매에 처방할 수 있는 약제로 acetylcholine 생성을 촉진하는 콜린 전구물질 (acetyl-L-carnitine hydrochloride, choline alfoscerate, nicergoline, oxiracetame)이 있다.
이들 약제들은 보험급여 인정을 받기 위해 특별한 검사를 하지 않아도 되기 때문에 처방이 용이하다. 특히 choline alfoscerate는 BBB (blood-brain barrier) 통과율이 45%로 뇌 부위에 고농도로 분포할 수 있고,BBB를 통과하여 혈중 농도의 45%가 뇌에 분포하는 것으로 알려져 있으며, 우울증으로 인한 가성 치매 및 노인 초기 우울증 치료에도 처방한다는 장점이 있다. 개인적으로 환자마다 약제에 대한 반응이 모두 다르기 때문에 4가지 콜린 전구물질을 모두 사용하면서, 3개월마다 문진이나 MMSE를 통해 반응평가를 하면서 처방을 조절한다.
그 외 은행잎 제제 (ginko biloba), 비타민 E, 에스트로겐, NSAID, 엽산 등과 같은 제제도 치매 치료에 처방되고 있지만 근거는 부족하다. 이에 비해 콜린 전구물질의 효과를 지지하는 논문들은 다수가 있으므로, 환자 상태 및 치료반응에 따라 적절한 제제를 선택하여 처방하면 되겠다. 또한 최근 발표된 ASCOMALVA 연구의 중간분석 결과에서 알 수 있듯이 cholinesterase 억제제 (donepezil)와 콜린 전구물질 (choline alfoscerate) 병용요법은 이들 제제의 단독요법에 비해 알츠하이머병 치료에 효과적이므로, 초기 치매를 지나서 중증으로 진행되는 환자에게는 부작용이 심한 donepezil 증량 대신 choline alfoscerate를 추가하는 전략을 고려하고 있다.
제2형 당뇨병과 치매
저혈당증으로 인해 뇌손상이 동반된 제2형 당뇨병 환자의 뇌 MRI 소견을 보면, 혈압과 혈당에 민감한 부위 (hippocampal area, temporal area, cerebral cortex, substantia nigra, basal ganglia)가 모두 손상된 것을 확인할 수 있다. 또한 저혈당증은 염증 마커를 증가시켜 혈관 내피세포 및 혈액응고 과정도 손상시키기 때문에 과연 엄격한 혈당조절이 유익한지에 대해 다시 한번 생각해볼 필요가 있으며, 이를 지지하는 논문도 계속해서 발표되고 있다(JAMA 2009;301(15):1565-72).
제2형 당뇨병의 일차 치료제로 널리 처방되는 메트포민은 렛트를 대상으로 한 동물실험에서 세포 증식 및 신경모세포 분화 감소를 정상화시켜 신경 손상을 감소시키는 것으로 알려졌다. 또한 GLP-1 유사체는 말초 인슐린 신호전달을 개선시켜 알츠하이머병 모델에서 인지기능 감소를 억제하며, DPP-4 억제제는 GLP-1 농도상승 및 β-amyloid, tau 감소를 통해 신경보호 효과를 나타낼 수 있는 것으로 알려졌다. 마지막으로 SGLT-2의 강력한 이중 억제제인 dapagliflozin 또한 acetylcholinesterase를 억제할 수 있어 알츠하이머병의 치료 표적으로 주목 받고 있다.
Discussion
좌장(김성래): 궁금하신 점은 자유롭게 질문하시기 바란다.

목지원: 외래에서 시행한 KDSQ (Korean Dementia Screening Questionnaire)에서 점수가 높으면 신경과로 진료의뢰를 하여 MMSE나 전문적인 검사를 받도록 한다. 그런데 6점 이상이어도 실제 MMSE 평가에서 심각한 문제는 없기 때문에 MCI로 진단하고 치료하고 있다. 그러나 피질하 혈관성 치매는 좀더 주의해서 치료할 필요가 있다고 생각된다.
박경선: 그래서 항혈소판제를 처방하기도 한다.
손장원: 그러하면 근거에 기반하여 어떤 제제를 처방하는 것이 가장 좋은가?
조광욱: 아스피린은 뇌졸중 이차 예방에 대해서만 근거가 있다. 일차 예방에 근거가 있는 제제가 현재로서는 없지만, 경험적으로 아스피린을 많이 처방하고 있다. 약물요법보다는 고지혈증이나 고혈압, 당뇨병과 같은 위험인자 관리가 더 중요하며, MCI인 경우에는 여러 과에서 치료를 받게 하는 것보다는 choline alfoscerate같은 콜린 전구물질을 처방에 추가하는 방법으로 치료하는 것이 훨씬 더 효과적일 수 있다.
김조은: 경증일 때는 확실히 효과가 있다. 처방 후 추적검사에서 50% 이상의 개선 효과를 보인다.
조광욱: 노인 환자에게는 의료진이 치료에 대한 믿음을 주는 것도 중요하다. 위약 효과처럼 별 것 아니지만 실제적인 효과로 나타날 때가 있다.
좌장(김성래): 고령이기도 하지만 당뇨병으로 인해 저혈당을 여러 번 경험한 환자들은 인지기능 감소를 보인다. 과거에는 어쩔 수 없는 증상으로 간과했지만 이제는 적극적인 약물치료도 고려할 필요가 있다.

